
Энергетика химических процессов
Категория реферата: Биология и химия
Теги реферата: скачать конспект урока, банк курсовых
Добавил(а) на сайт: Канаев.
Предыдущая страница реферата | 1 2 3 4 5 6 7
![]() известны для немногих соединений, но вместе с
тем с помощью
известны для немногих соединений, но вместе с
тем с помощью ![]()
![]() и
и ![]() можно вычислить
можно вычислить ![]() для десятков тысяч реакций, в том числе
предполагаемых и не изученных экспериментально.
для десятков тысяч реакций, в том числе
предполагаемых и не изученных экспериментально.
В складских помещениях сосредоточены большие количества разнообразных по ассортименту и физико–химическим (в том числе и пожароопасным) свойствам веществ. При нарушении правил хранения возможно образование смесей, способных к экзотермическим реакциям. Такие смеси представляют значительную пожарную опасность. Одни смеси, образованные при контакте негорючего окислителя с горючим, самовозгораются (KMnO4+глицерин; CrO3+ацетон). Другие смеси воспламеняются или взрываются от удара, трения или нагревания (KClO3+сера). Третьи смеси, образованные из негорючих компонентов, при взаимодействии нагревается от теплоты реакции (CaO+вода) или взрываются (KClO3+H2SO4).
Пожарную
опасность веществ и их смесей можно определить по энергии Гиббса ![]() , которая
является мерой реакционной способности веществ. Как было показано ранее, реакции между веществами, сопровождающиеся большой потерей энергии Гиббса, протекают самопроизвольно и до конца, иногда приобретают взрывной характер. В
этих реакциях энергия Гиббса отрицательна, то есть в исходном состоянии системы
(реагирующих веществ) она больше, чем в конечном (продуктов реакции).
, которая
является мерой реакционной способности веществ. Как было показано ранее, реакции между веществами, сопровождающиеся большой потерей энергии Гиббса, протекают самопроизвольно и до конца, иногда приобретают взрывной характер. В
этих реакциях энергия Гиббса отрицательна, то есть в исходном состоянии системы
(реагирующих веществ) она больше, чем в конечном (продуктов реакции).
Ориентировочно
за величину, определяющую направленность процесса, принимают значение 41,8
кДж/моль. Если для реакции расчетом получено ![]() , то реакция
возможна не только в стандартных, но и в нестандартных условиях.
, то реакция
возможна не только в стандартных, но и в нестандартных условиях.
Если
![]() , то процесс
невозможен как в стандартных, так и в иных условиях. По изменению энергии
Гиббса от -41,8 до 41,8 кДж/моль нельзя сделать заключения о возможности
протекания процесса в стандартных условиях, но вещества относятся к
пожароопасным, хотя эти свойства у них появляются в условиях, отличных от
стандартных (например, во время пожара).
, то процесс
невозможен как в стандартных, так и в иных условиях. По изменению энергии
Гиббса от -41,8 до 41,8 кДж/моль нельзя сделать заключения о возможности
протекания процесса в стандартных условиях, но вещества относятся к
пожароопасным, хотя эти свойства у них появляются в условиях, отличных от
стандартных (например, во время пожара).
Если
для веществ по расчету получено ![]() , то вещества, участвующие в реакции, пожароопасны и несовместимы. К совместному хранению
такие вещества не допускаются. При
, то вещества, участвующие в реакции, пожароопасны и несовместимы. К совместному хранению
такие вещества не допускаются. При ![]() вещества совместимые и допускаются к
совместному хранению.
вещества совместимые и допускаются к
совместному хранению.
Возможность использования энергии Гиббса для оценки пожарной опасности вещества подтверждается следующими примерами.
Пример 1. Определить пожарную опасность разложения твердого окислителя KMnO4 при нагревании. Разложение вещества идет по схеме:
2KMnO4 Þ K2MnO4 + MnO2 + O2.
Решение.
Из справочника термодинамических величин находим ![]() веществ, кДж/моль:
веществ, кДж/моль:
![]() KMnO4 –
729,6
KMnO4 –
729,6
K2MnO4 – 1169,2
MnO2 – 467
Находим
![]() :
:
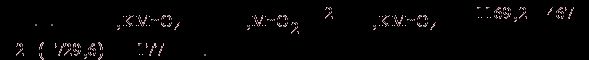 -88,5 кДж/моль
< - 41,8 кДж/моль – процесс разложения KMnO4 идет самопроизвольно.
-88,5 кДж/моль
< - 41,8 кДж/моль – процесс разложения KMnO4 идет самопроизвольно.
Практически разложение марганцовки при стандартных условиях не происходит. Несмотря на это, KMnO4 следует считать пожароопасным веществом, так как при 240 °С процесс становится самопроизвольным и активным, с выделением О2, что представляет пожарную опасность.
Пример 2. Установить пожарную опасность контакта негорючего CrO3 с горючей жидкостью ацетоном.
3C3H6O + 16CrO3 Þ 8Cr2O3 + 9CO2 + 9H2O
Решение:
Находим из справочника ![]() , кДж/моль:
, кДж/моль:
CrO3 ï – 513,8 кДж/моль
Cr2O3 ï – 1059,7 кДж/моль
Ацетон ï – 155,5 кДж/моль
CO2 ï – 394,6 кДж/моль
H2O(г) ï – 237,4 кДж/моль
![]() = 8(-1059,7) +
9(-237,4) + 9 (-394,6) - 3(-155,5) - 16(-513,8) = -5478,3 кДж.
= 8(-1059,7) +
9(-237,4) + 9 (-394,6) - 3(-155,5) - 16(-513,8) = -5478,3 кДж.
Из расчета на один моль ацетона: -1826,1 кДж/моль < - 41,8 кДж/моль – возможен самопроизвольный процесс в стандартных условиях.
Эксперимент показывает, что контакт этих веществ приводит к самовозгоранию и взрыву. Следовательно, совместное хранение этих веществ с точки зрения пожарной безопасности недопустимо.
Список литературы
Глинка Н.Л. Общая химия. – М.: Химия, 1978. – С. 183-201.
Карапетьянц М.Х. Введение в теорию химических процессов. – М.:
Высшая школа, 1981. – С. 7-75
Шиманович И.В., Павлович М.Л., Тикавый П.Ф., Малашко П.М. Общая химия в формулах, определениях, схемах. – Мн.: Унiверсiтэцкае, 1996. – С. 89-102.
Кудрявцев А.А. Составление химических уравнений. – М.: Высшая школа, 1991. – 264 С.
Воробьев В.К., Елисеев С.Ю., Врублевский А.В. Практические и самостоятельные работы по химии. – Мн.: УП «Донарит», 2005. – С. 30-39.
Скачали данный реферат: Янаслов, Marionilla, Jurasov, Манин, Савасин, Sabitov.
Последние просмотренные рефераты на тему: диплом купить, сочинения по русскому языку, организация реферат, реферат республика беларусь.
Предыдущая страница реферата | 1 2 3 4 5 6 7