
Химическая кинетика и равновесие в гомогенных системах
Категория реферата: Биология и химия
Теги реферата: доклады о животны, реферати
Добавил(а) на сайт: Колвецкий.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата
Если бы каждое столкновение приводило к акту взаимодействия, все реакции должны были бы протекать со скоростью взрыва. На самом деле к актам взаимодействия приводит лишь незначительное число столкновений. К реакции приводят столкновения только активных молекул, запас энергии которых достаточен для совершения элементарного акта реакции. Число активных соударений при данной температуре пропорционально общему содержанию реагирующих молекул. С ростом температуры число активных соударений возрастает гораздо сильнее, чем общее число столкновений.
Для того, чтобы при столкновении молекулы успели прореагировать, химические связи должны быть «расшатаны». Для этого молекула должна обладать повышенным запасом энергии. Молекулы, обладающие этим необходимым запасом энергии, называются активированными. При нагревании веществ активизация молекул происходит благодаря ускорению их поступательного движения, а также вследствие усиления колебательного движения атомов и атомных групп в самих молекулах. Все это приводит к ослаблению связей внутри молекул. Таким образом, для того, чтобы молекулы прореагировали, им необходимо преодолеть некоторый энергетический барьер.
В соответствии с изложенным изменение энергии системы А+В при ее превращении в S может быть графически представлено следующим образом (рис. 5.4.)
Молекула S образуется из А и В в результате перераспределения атомов и химических связей. Для образования молекулы S активированные молекулы А и В при столкновении вначале образуют активированный комплекс АВ, внутри которого и происходит перераспределение атомов. Энергия, необходимая для возбуждения молекулы до энергии активирования комплекса, называется энергией активации Еа.
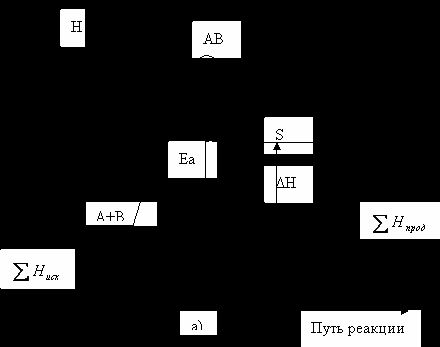
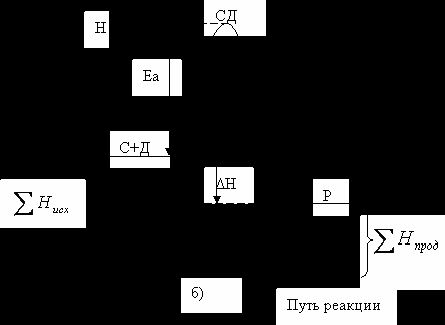
Рис. 5.4. Диаграмма изменения энтальпий для эндотермических (а)
и экзотермических (б) процессов.
На
рисунке а) видно, что продукты реакции обладают большим запасом энергии, чем
исходные вещества, то есть реакция А + В ® S эндотермическая.
Разность между энергией продуктов реакции и исходных веществ является тепловым
эффектом реакции ![]() .
.
Соответствующий график для экзотермической реакции С + Д → Р представлен на рисунке б).
Взаимосвязь между константой скорости реакции k и энергией активации Еа определяется уравнением Аррениуса:
 ,
,
где А – предэкспоненциальный коэффициент, связанный с вероятностью и числом столкновений.
Логарифмирование уравнения Аррениуса:
 или
или 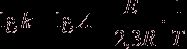
дает уравнение прямой линии. Знание констант скорости при нескольких температурах позволяет определить энергию активации данной реакции:
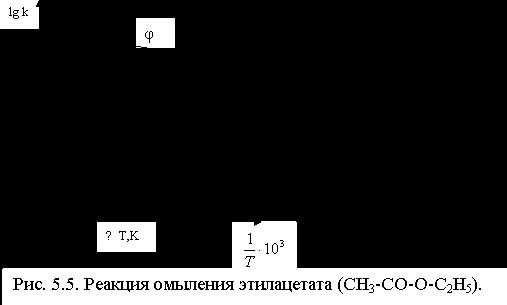
Тангенс угла наклона этой прямой к оси абсцисс равен:
 .
.
Энергия активации является тем фактором, посредством которого природа реагирующих веществ влияет на скорость химической реакции.
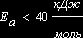 - «быстрые» реакции (ионные реакции в
растворах);
- «быстрые» реакции (ионные реакции в
растворах);
 - реакции с измеряемой скоростью
- реакции с измеряемой скоростью
(Н2SO4 + Na2S2O3 = Na2SO4 + SO2 + S + H2O);
 - «медленные» реакции
- «медленные» реакции
(синтез NH3 при обычных температурах).
Рекомендуем скачать другие рефераты по теме: доклад на тему физика, реферат на тему жизнь.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата