Химические элементы в организме человека
Категория реферата: Биология и химия
Теги реферата: реферати українською, скачать бесплатно конспекты
Добавил(а) на сайт: Pavlina.
Предыдущая страница реферата | 1 2 3 4 5 6 7 | Следующая страница реферата
Рефераты | Биология и химия | Химические элементы в организме человека
Химические элементы в организме человекаКатегория реферата: Биология и химия Теги реферата: реферати українською, скачать бесплатно конспекты Добавил(а) на сайт: Pavlina. Предыдущая страница реферата | 1 2 3 4 5 6 7 | Следующая страница реферата |
800-1200 |
210 |
|
|
SO42- |
10 |
- |
|
|
I |
0,15 |
0,07 |
|
|
Se |
0,05-0,07 |
- |
|
|
F |
1,5-4,0 |
0,6 |
Несомненно, время внесет коррективы в современные представления о числе и биологической роли определенных химических элементов в организме человека. В данной статье мы будем исходить из того, что уже достоверно известно. Роль макроэлементов, входящих в состав неорганических веществ, очевидна. Например, основное количество кальция и фосфора входит в кости (гидроксофосфат кальция Ca10(PO4)6(OH)2), а хлор в виде соляной кислоты содержится в желудочном соке.
Микроэлементы вошли в отмеченный выше ряд 22 элементов, обязательно присутствующих в организме человека. Заметим, что большинство из них - металлы, а из металлов больше половины являются d-элементами. Последние в организме образуют координационные соединения со сложными органическими молекулами. Так, установлено, что многие биологические катализаторы - ферменты содержат ионы переходных металлов (d-элементов). Например, известно, что марганец входит в состав 12 различных ферментов, железо - в 70, медь - в 30, а цинк - более чем в 100. Микроэлементы называют жизненно необходимыми, если при их отсутствии или недостатке нарушается нормальная жизнедеятельность организма. Характерным признаком необходимого элемента является колоколообразный вид кривой доза (n) - ответная реакция (R, эффект) (рис. 1).
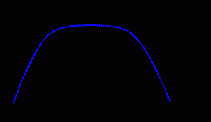
Рис. 1. Зависимость ответной реакции (R) от дозы (n) для жизненно необходимых элементов
При малом поступлении данного элемента организму наносится существенный ущерб. Он функционирует на грани выживания. В основном это объясняется снижением активности ферментов, в состав которых входит данный элемент. При повышении дозы элемента ответная реакция возрастает и достигает нормы (плато). При дальнейшем увеличении дозы проявляется токсическое действие избытка данного элемента, в результате чего не исключается и летальный исход. Кривую на рис. 1 можно трактовать так: все должно быть в меру и очень мало и очень много вредно. Например, недостаток в организме железа приводит к анемии, так как оно входит в состав гемоглобина крови, а точнее, его составной части - гема. У взрослого человека в крови содержится около 2,6 г железа. В процессе жизнедеятельности в организме происходят постоянный распад и синтез гемоглобина. Для восполнения железа, потерянного с распадом гемоглобина, человеку необходимо суточное поступление в организм с пищей в среднем около 12 мг этого элемента. Связь анемии с недостатком железа была известна врачам давно, так как еще в XVII веке в некоторых европейских странах при малокровии прописывали настой железных опилок в красном вине. Однако избыток железа в организме тоже вреден. С ним связан сидероз глаз и легких - заболевания, вызываемые отложением соединений железа в тканях этих органов. Главный регулятор содержания железа в крови - печень.
Недостаток в организме меди приводит к деструкции кровеносных сосудов, патологическому росту костей, дефектам в соединительных тканях. Кроме того, считают, что дефицит меди служит одной из причин раковых заболеваний. В некоторых случаях поражение легких раком у людей пожилого возраста врачи связывают с возрастным снижением содержания меди в организме. Однако избыток меди в организме приводит к нарушению психики и параличу некоторых органов (болезнь Вильсона). Человеку причиняют вред лишь относительно большие количества соединений меди. В малых дозах их используют в медицине как вяжущее и бактериостазное (задерживающее рост и размножение бактерий) средство. Так, например, сульфат меди (II) применяют при лечении конъюктивитов в виде глазных капель (25%-ный раствор), а также для прижиганий при трахоме в виде глазных карандашей (сплав сульфата меди(II), нитрата калия, квасцов и камфоры). При ожогах кожи фосфором проводят ее обильное смачивание 5%-ным раствором сульфата меди (II).
Таблица 2. Характерные симптомы дефицита химических элементов в организме человека
|
Дефицит элемента |
Типичный симптом |
||||
|
Ca |
Замедление роста скелета Рекомендуем скачать другие рефераты по теме: диплом работа, реферат влияние. Предыдущая страница реферата | 1 2 3 4 5 6 7 | Следующая страница реферата Поделитесь этой записью или добавьте в закладкиКатегории: |