
Моделирование состава жидких фармформ на основе азотсодержащих органических трииодидов
Категория реферата: Биология и химия
Теги реферата: мировая экономика, реферат китай курсовые работы
Добавил(а) на сайт: Kaufman.
1 2 | Следующая страница реферата
Моделирование состава жидких фармформ на основе азотсодержащих органических трииодидов с учетом влияния иодкоординирующего растворителя
Е.Б. Подгорная, М.С. Черновьянц, А.И. Пыщев, Ростовский государственный университет
Известно, что иодсодержащие соединения обладают высокой антимикробной и антивирусной активностью [1]. Синтезированы новые биологически активные соединения - трииодиды азотсодержащих органических катионов: 1,3-диметилбензимидазолия (I), 1,3-диэтилбензимидазолия (II), N-децилпиридиния (III), N-цетилпиридиния (IV), N-метилуротропиния (V), тетраэтиламмония (VI). Сочетание биологической активности иодсодержащих соединений и токсичности свободного иода делает необходимым точное установление формы существования иода в составе органических азотсодержащих соединений. Подбор оптимальных условий синтеза с учетом влияния иодкоординирующего растворителя позволит прогнозировать образование биологически активных форм с заданной способностью освобождать молекулярный иод.
На основании спектрофотометрического исследования равновесия KtI+nI2 = KtI2n+1 в хлороформных растворах сделана оценка предельного количества молекул иода, координируемых иодидами азотсодержащих органических катионов: одна - для иодидов производных бензимидазолия и тетраэтиламмония с образованием структуры KtI3 и две - для иодидов трех остальных катионов с образованием структуры KtI5. Впервые для расчета констант устойчивости полииодиодидов предложена функция nI2 - среднеиодное число [2]. Найденные значения констант устойчивости органических трииодидов (1) и пентаиодидов (2) позволяют рассчитать мольные доли продуктов взаимодействия иода с иодидами I-VI от концентрации свободного иода в хлороформной среде по уравнению:
ф = А / (1 + 1 [I2] + 2 [I2]2),
где А = 1 для KtI; A = 1 [I2] для трииодидов; A = 2 [I2] для пентаиодидов.
Концентрация свободного иода определялась спектрофотометрически для каждого значения аналитической концентрации иода (СI2) по индивидуальной полосе поглощения иода, выделенной из суммарной спектральной кривой методом традиционного нелинейного регрессионного анализа [3]. Кривые распределения для систем II - I (а) и III - I (б) представлены на рис. 1.
Зависимости мольных долей образующихся органических трииодидов и пентаиодидов в хлороформной среде от концентрации иода предоставляют возможность подобрать оптимальные условия синтеза трииодидов I-VI при минимальной примеси иодида и пентаиодида.
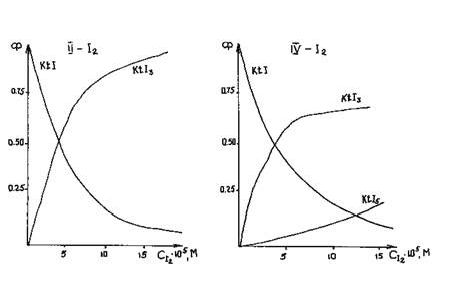
Рис.1. Кривые распределения продуктов взаимодействия иода с органическими азотсодержащими иодидами в хлороформной среде CKtI = 5 ·10-5 моль/л.
|
CII, моль/л |
ФII в ДМСО |
ФII в этаноле |
|
3,6.10-1 1,0.10-2 1,0.10-3 1,0.10-4 |
0,96 0,80 0,50 0,15 |
0,99 0,92 0,76 0,43 |
Мольные доли субстанции II в растворе для различных растворяемых концентраций.
Рекомендуем скачать другие рефераты по теме: курсовые работы бесплатно, мировая экономика.
1 2 | Следующая страница реферата