
Теория окислительно-восстановительных реакций
Категория реферата: Биология и химия
Теги реферата: реферат на тему образ жизни, контроль реферат
Добавил(а) на сайт: Килиц.
1 2 | Следующая страница реферата
Теория окислительно-восстановительных реакций
После открытия кислорода, французскому химику Лавуазье удалось выяснить, что горение есть реакция соединения с кислородом. В соответствии латинским наименованием кислорода "oxigenium" реакции соединения с кислородом были названы окислением.
2Mg0 +O20=2Mg+2O-2
Обратный процесс полного или частичного отнятия кислорода от веществ называется восстановлением. При восстановлении оксида элемент, соединённый с кислородом, меняет своё состояние - образует простое вещество, т.е. восстанавливается.
Fe2+3O3-2+2Al0=Al2+3O3-2+2Fe0
Вы заметили, что в этих реакциях изменились степени окисления химических элементов. Химические реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вешества, называют окислительно-восстановительными реакциями.
В соответствиии с теорией электронного строения атома окисление и восстановление легко объясняется как процесс отдачи или присоединения электронов. В окислительно-восстановительных реакциях электроны не уходят из сферы реакции, а переносятся от одного элемента к другому.
Рассмотрим реакцию взаимодействия магния с кислородом.
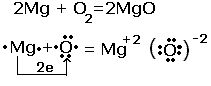
Из схемы видно, что атом магния отдал 2 электрона атому кислорода, за счёт такого перехода химические элементы изменили степени окисления. Протекают два процесса. Процесс отдачи электронов и процесс их присоединения , которые называются соответственно окислением и восстановлением.
Вещества, участвующие в окислительно-восстановительных реакциях, и у которых изменились степени окисления, являются либо окислителямия,либо восстановителями.
Окислитель - это атомы, ионы или молекулы, которые принимают электроны.
Восстановитель - это атомы, ионы или молекулы, которые отдают электроны.
Из уравнения реакции видно, что магний является восстановителем, а кислород - окислителем.
|
Запомните! Восстановитель в химической реакции всегда окисляется, окислитель - восстанавливается. |
Важнейшие восстановители и окислители.
|
Восстановители |
Окислители |
||||
|
Металлы, водород, уголь |
Фтор, хлор, бром, иод |
||||
|
Оксид углерода (II) CO |
Перманганат калия KMnO4, манганат калия K2MnO4, оксид марганца (IV)MnO2 |
||||
|
Сероводород H2Sоксид серы (IV)SO2 |
Бихромат калия K2Cr2O7, хромат калия K2CrO4 |
||||
|
HI, HBr, HCl |
Азотная кислота HNO3 Рекомендуем скачать другие рефераты по теме: шпоры для студентов, доклад по биологии. 1 2 | Следующая страница реферата Поделитесь этой записью или добавьте в закладкиКатегории: |