
Водные растворы электролитов
Категория реферата: Биология и химия
Теги реферата: скачать реферат, банк курсовых работ бесплатно
Добавил(а) на сайт: Владимира.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата
так как процесс диссоциации является эндотермическим, то степень диссоциации слабого электролита в водных растворах будет увеличиваться с повышением температуры.
Константой электролитической диссоциации К называется постоянная химического равновесия в растворе электролита:
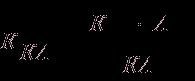 ,
,
где
[К+], [A-] и [KA] - концентрации в растворе ионов ![]() и
и ![]() (в г-ион/л) и недиссоциированного соединения
КА (в моль/л).
(в г-ион/л) и недиссоциированного соединения
КА (в моль/л).
Чем больше К, тем электролит лучше распадается на ионы. Для данного электролита значение К постоянно при определенной температуре и в отличие от a не зависит от концентрации.
Связь между константой К и степенью диссоциации a может быть найдена следующим образом. Концентрация ионов К+ и А- в растворе равна
[К+] = [А-] = aС,
где С – исходная молярная концентрация; a – степень электролитической диссоциации электролита. Концентрация недиссоциировавших молекул КА в растворе равна
[КА]=(1- a)С.
Откуда
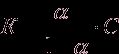 .
.
Данное уравнение выражает закон разбавления Оствальда.
Если a мала, то 1- a ≈ 1 и тогда
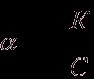 .
.
Видно, что с уменьшением концентрации электролита в растворе степень электролитической диссоциации возрастает.
Диссоциация слабого электролита, молекула которого может диссоциировать не на два, а на большее количество ионов (электролиты с разновалентными ионами), протекает по стадиям (ступенчатая диссоциация). Например, при диссоциации слабой угольной кислоты Н2СО3 в водном растворе имеют место следующие равновесия:
I стадия: Н2СО3 <=> Н+ + НСО3-
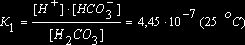 .
.
II стадия: НСО3- <=> Н+ + СО32-
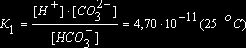 .
.
Как видно из этих данных, процесс диссоциации слабого электролита с разновалентными ионами определяется главным образом первой ступенью.
Для примера приведем константы электролитической диссоциации некоторых слабых кислот и оснований (25 °С):
|
СН3СООН |
<=> |
H+ + CH3COO- |
1,76·10-5 Рекомендуем скачать другие рефераты по теме: рынок реферат, новшество. Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата Поделитесь этой записью или добавьте в закладкиКатегории: |