
Билеты по химии 10 класс
Категория реферата: Рефераты по науке и технике
Теги реферата: выборы реферат, решебник по математике 6 виленкин
Добавил(а) на сайт: Gershel'man.
Предыдущая страница реферата | 2 3 4 5 6 7 8 9 10 11 12 | Следующая страница реферата
![]()
2) в результате реакции выделяется газ:
![]()
3) в результате реакции образуется малодиссоциирующее вещество:
![]()
Ионный обмен – это процесс, в результате которого ионы, находящиеся в твердой фазе. обмениваются с ионами, находящимися в растворе. Нерастворимое твердое вещество может представлять собой какой-либо природный материал либо синтетическую смолу. Природные материалы, используемые для ионного обмена, включают цеолиты (комплексные алюмосиликаты натрия) и глауконитовый песок.
На поверхности этих твердых веществ имеются электрически заряженные центры, расположенные на более или менее регулярном расстоянии друг от друга. Эти центры удерживают на себе простые ионы с зарядами противоположного знака. Именно эти ионы обмениваются с другими ионами, содержащимися в растворе.
Катионообменники. Катионообменные материалы состоят из трех частей:
1) основная масса, или скелет, обычно обозначаемый символом R–;
2) активные центры (такие группы, как —![]() либо —
либо —![]() );
);
3) катионы, подлежащие обмену (обычно это ионы Н+ или Н3О+).
Когда твердый катионообменник приходит в соприкосновение с раствором, в котором содержатся какие-либо ионы, между ними устанавливается равновесие. Например,
![]()
Если первоначально раствор содержит, например, хлорид натрия, то ионы натрия обмениваются с ионами водорода и из нижней части колонки вытекает разбавленный раствор соляной кислоты.
Ионообменный материал можно регенерировать (восстанавливать), промывая колонку разбавленной соляной кислотой. Это приводит к смещению влево рассматриваемого равновесия, в результате чего ионы натрия замещаются ионами водорода.
Анионообменники. Анионообменник удаляет из раствора анионы. Типичным примером анионного обмена является следующее равновесие:
![]()
Для регенерации анионообменника может использоваться какое-либо основание, например раствор гидроксида натрия. Это сдвигает указанное равновесие влево.
Билет №8.Скорость химических реакций. Факторы, влияющие на скорость химической реакции (зависимость скорости от природы, концентрации вещества, площади поверхности соприкосновения реагирующих веществ, температуры, катализатора).
Скоростью химической реакции называется изменение количества вещества за единицу времени в единице объема.
![]()
Скорость реакции зависит от природы реагирующих веществ.
При реакции металлов с соляной кислотой, чем левее расположен металл в раду напряжений, тем быстрее протекает реакция, а металлы, находящиеся правее водорода, не реагируют вообще:
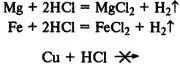
Скорость реакции увеличивается при увеличении концентрации реагирующих веществ.
Рекомендуем скачать другие рефераты по теме: шпаргалки по педагогике, доклад по обж.
Предыдущая страница реферата | 2 3 4 5 6 7 8 9 10 11 12 | Следующая страница реферата