
Молекулярная физика
Категория реферата: Рефераты по науке и технике
Теги реферата: страхование реферат, сообщение об открытии
Добавил(а) на сайт: Venedikta.
1 2 3 4 5 6 7 | Следующая страница реферата
Молекулярно-кинетическая теория – учение о строении и свойствах вещества, использующее представление о существовании атомов и молекул как наименьших частиц химического вещества. В основе МКТ лежат три строго доказанных с помощью опытов утверждения:
Вещество состоит из частиц – атомов и молекул, между которыми существуют промежутки; Эти частицы находятся в хаотическом движении, на скорость которого влияет температура; Частицы взаимодействуют друг с другом.То, что вещество действительно состоит из молекул, можно доказать, определив их размеры: Капля масла расплывается по поверхности воды, образуя слой, толщина которого равна диаметру молекулы. Капля объемом 1 мм3 не может расплыться больше, чем на 0,6 м2:
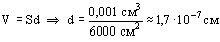
Существуют также другие способы доказательства существования молекул, но перечислять их нет необходимости: современные приборы (электронный микроскоп, ионный проектор) позволяют видеть отдельные атомы и молекулы.
Силы взаимодействия молекул. а) взаимодействие имеет электромагнитный характер; б) силы короткодействующие, обнаруживаются на расстояниях, сопоставимых с размерами молекул; в) существует такое расстояние, когда силы притяжения и отталкивания равны (R0), если R>R0, тогда преобладают силы притяжения, если R<R0 – силы отталкивания.
Действие сил молекулярного притяжения обнаруживается в опыте со свинцовыми цилиндрами, слипающимися после очистки их поверхностей.
Молекулы и атомы в твердом теле совершают беспорядочные колебания относительно положений, в которых силы притяжения и отталкивания со стороны соседних атомов уравновешены. В жидкости молекулы не только колеблются около положения равновесия, но и совершают перескоки из одного положения равновесия в соседнее, эти перескоки молекул являются причиной текучести жидкости, ее способности принимать форму сосуда. В газах обычно расстояния между атомами и молекулами в среднем значительно больше размеров молекул; силы отталкивания на больших расстояниях не действуют, поэтому газы легко сжимаются; практически отсутствуют между молекулами газа и силы притяжения, поэтому газы обладают свойством неограниченно расширяться.
Масса и размер молекул. Постоянная Авогадро:Любое вещество состоит из частиц, поэтому количество вещества принято считать пропорциональным числу частиц. Единицей количества вещества является моль. Моль равен количеству вещества системы, содержащей столько же частиц, сколько содержится атомов в 0,012 кг углерода.
Отношение числа молекул к количеству вещества называется постоянной Авогадро:
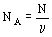
Постоянная Авогадро равна 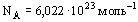 . Она показывает, сколько атомов или молекул содержится в одном моле вещества.
. Она показывает, сколько атомов или молекул содержится в одном моле вещества.
Количество вещества можно найти как отношение числа атомов или молекул вещества к постоянной Авогадро:
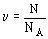
Молярной массой называется величина, равная отношению массы вещества к количеству вещества:
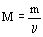
Молярную массу можно выразить через массу молекулы:
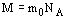
Для определения массы молекул нужно разделить массу вещества на число молекул в нем:
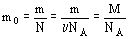
Броуновское движение – тепловое движение взвешенных в газе или жидкости частиц. Английский ботаник Роберт Броун (1773– 1858) в 1827 году обнаружил беспорядочное движение видимых в микроскоп твердых частиц, находящихся в жидкости. Это явление было названо броуновским движением. Это движение не прекращается; с увеличением температуры его интенсивность растет. Броуновское движение– результат флуктуации давления (заметного отклонения от средней величины).
Причина броуновского движения частицы заключается в том, что удары молекул жидкости о частицу не компенсируют друг друга.
Идеальный газ:У разреженного газа расстояние между молекулами во много раз превышает их размеры. В этом случае взаимодействие между молекулами пренебрежимо мало и кинетическая энергия молекул много больше потенциальной энергии их взаимодействия.
Для объяснения свойств вещества в газообразном состоянии вместо реального газа используется его физическая модель- идеальный газ. В модели предполагается:
расстояние между молекулами чуть больше их диаметра; молекулы – упругие шарики; между молекулами не действуют силы притяжения; при соударении молекул друг с другом и со стенками сосуда действуют силы отталкивают; движения молекул подчиняется законам механики. Основное уравнение МКТ идеального газа:Основное уравнение МКТ позволяет вычислить давление газа, если известны масса молекулы, среднее значение квадрата скорости и концентрация молекул.
Давление идеального газа заключается в том, что молекулы при столкновениях со стенками сосуда взаимодействуют с ними по законам механики как упругие тела. При столкновении молекулы со стенкой сосуда проекция скорости vx вектора скорости на ось OX, перпендикулярную стенке, изменяет свой знак на противоположный, но остается постоянной по модулю. Поэтому в результате столкновений молекулы со стенкой проекция ее импульса на ось OX изменяется от mv1x=-mvx до mv2x=mvx. Изменение импульса молекулы при столкновении со стенкой вызывает сила F1, действующая на нее со стороны стенки. Изменение импульса молекулы равно импульсу этой силы:
Рекомендуем скачать другие рефераты по теме: пожары реферат, ответы 5 класс.
1 2 3 4 5 6 7 | Следующая страница реферата