
Фосфор и его соединения
Категория реферата: Биология и химия
Теги реферата: курсовики скачать бесплатно, шпаргалки по химии
Добавил(а) на сайт: Фёдоров.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата
Рефераты | Биология и химия | Фосфор и его соединения
Фосфор и его соединенияКатегория реферата: Биология и химия Теги реферата: курсовики скачать бесплатно, шпаргалки по химии Добавил(а) на сайт: Фёдоров. Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата |
44,1 |
280,5 |
Белый кристаллический порошок, ядовит, самовозгорается на воздухе. При 280—300°С переходит в красный |
|
|
Красный |
2,3 |
590 |
Возгоняется около 400°С |
Красный кристаллический или аморфный порошок, неядовит. При 220°С и 12 × 108 Па переходит в черный фосфор. Загорается на воздухе только при поджигании |
|
Черный |
2,7 |
При нагревании переходит в красный фосфор |
Графитоподобная структура. При нормальных условиях — полупроводник, под давлением проводит электрический ток как металл |
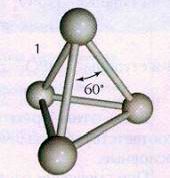 Белая модификация фосфора, получающаяся при конденсации
паров, имеет молекулярную кристаллическую решетку, в узлах которой
дислоцированы молекулы Р4 (рис.1). Из-за слабости межмолекулярных сил белый
фосфор летуч, легкоплавок, режется ножом и растворяется в
неполярных растворителях, например в сероуглероде. Белый фосфор весьма
реакционноспособное вещество. Он энергично взаимодействует с кислородом, галогенами, серой и металлами. Окисление фосфора на воздухе сопровождается
разогреванием и свечением. Поэтому белый фосфор хранят под водой, с которой он
не реагирует. Белый фосфор очень токсичен.
Белая модификация фосфора, получающаяся при конденсации
паров, имеет молекулярную кристаллическую решетку, в узлах которой
дислоцированы молекулы Р4 (рис.1). Из-за слабости межмолекулярных сил белый
фосфор летуч, легкоплавок, режется ножом и растворяется в
неполярных растворителях, например в сероуглероде. Белый фосфор весьма
реакционноспособное вещество. Он энергично взаимодействует с кислородом, галогенами, серой и металлами. Окисление фосфора на воздухе сопровождается
разогреванием и свечением. Поэтому белый фосфор хранят под водой, с которой он
не реагирует. Белый фосфор очень токсичен.
Около 80% от всего производства белого фосфора идет на синтез чистой ортофосфорной кислоты. Она в свою очередь используется для получения полифосфатов натрия (их применяют для снижения жесткости питьевой воды) и пищевых фосфатов. Оставшаяся часть белого фосфора расходуется для создания дымообразующих веществ и зажигательных смесей.
Техника безопасности. В производстве фосфора и его соединений требуется соблюдение особых мер предосторожности, т.к. белый фосфор – сильный яд. Продолжительная работа в атмосфере белого фосфора может привести к заболеванию костных тканей, выпадению зубов, омертвению участков челюстей. Воспламеняясь, белый фосфор вызывает болезненные, долго не заживающие ожоги. Хранить белый фосфор следует под водой, в герметичных сосудах. Горящий фосфор тушат двуокисью углерода, раствором CuSO4 или песком. Обоженную кожу следует промыть раствором KmnO4 или CuSO4. Противоядием при отравлении фосфором является 2%-ый раствор CuSO4.
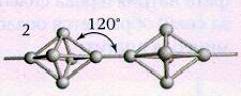 При длительном хранении, а также при нагревании белый
фосфор переходит в красную модификацию (впервые его получили лишь 1847 году).
Название красный фосфор относится сразу к нескольким модификациям, различающихся по плотности и окраске:
она колеблется от оранжевой до темно-красной и даже фиолетовой. Все
разновидности красного фосфора нерастворимы в органических растворителях, и по
сравнению с белым фосфором они менее реакционноспособны и имеют полимерное
строение: это тетраэдры Р4, связанные друг с другом в бесконечные цепи (рис.2).
При длительном хранении, а также при нагревании белый
фосфор переходит в красную модификацию (впервые его получили лишь 1847 году).
Название красный фосфор относится сразу к нескольким модификациям, различающихся по плотности и окраске:
она колеблется от оранжевой до темно-красной и даже фиолетовой. Все
разновидности красного фосфора нерастворимы в органических растворителях, и по
сравнению с белым фосфором они менее реакционноспособны и имеют полимерное
строение: это тетраэдры Р4, связанные друг с другом в бесконечные цепи (рис.2).
Красный фосфор находит применение в металлургии, производстве полупроводниковых материалов и ламп накаливания, используется в спичечном производстве.
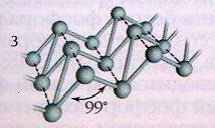 Наиболее стабильной модификацией фосфора является черный
фосфор. Его получают аллотропным превращением белого фосфора при t=2200C и повышенным давлением. По внешнему
виду он напоминает графит. Кристаллическая структура черного фосфора слоистая, состоящая из гофрированных слоев (рис.3). Черный фосфор – это наименее активная модификация фосфора. При
нагревании без доступа воздуха он, как и красный, переходит в пар, из которого
конденсируется в белый фосфор.
Наиболее стабильной модификацией фосфора является черный
фосфор. Его получают аллотропным превращением белого фосфора при t=2200C и повышенным давлением. По внешнему
виду он напоминает графит. Кристаллическая структура черного фосфора слоистая, состоящая из гофрированных слоев (рис.3). Черный фосфор – это наименее активная модификация фосфора. При
нагревании без доступа воздуха он, как и красный, переходит в пар, из которого
конденсируется в белый фосфор.
Оксид фосфора (V)
|
Фосфор образует несколько оксидов. Важнейшим из них является оксид фосфора (V) P4O10 (Рис.4). Часто его формулу пишут в упрощенном виде – P2O5. В структуре этого оксида сохраняется тетраэдрическое расположение атомов фосфора. |
|
P2+5O5 Фосфорный ангидрид (оксид фосфора (V))
Белые кристаллы, t0пл.= 5700С, t0кип.= 6000C, r = 2,7 г/см3. Имеет несколько модификаций. В парах состоит из молекул P4H10, очень гигроскопичен (используется как осушитель газов и жидкостей).
Получение
4P + 5O2 ® 2P2O5