
Химическая связь. Типы взаимодействия молекул
Категория реферата: Биология и химия
Теги реферата: зимой сочинение, новшество
Добавил(а) на сайт: Федосия.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 9 | Следующая страница реферата
Из квантовых ячеек N и Н можно видеть, что атом азота имеет 3
|
N |
¯ |
H |
||||||||||||||
|
2s |
2p |
1s |
неспаренных электрона, а атом водорода – один. Принцип насыщаемости указывает на то, что устойчивым соединением должен быть NH3, а не NH2, NH или NH4. Однако существуют молекулы, содержащие нечетное число электронов, например, NO, NO2, ClO2. Все они характеризуются повышенной реакционной способностью.
На отдельных стадиях химических реакций могут образовываться и валентно ненасыщенные группы, которые называются радикалами, например, H, NH2, O, CH3. Реакционная способность радикалов очень высока и поэтому время их существования, как правило, мало.
Донорно-акцепторный механизм
Известно, что валентно насыщенные соединения аммиак NH3 и трифторид бора BF3 реагируют друг с другом по реакции
NH3 + BF3 = NH3BF3 + 171,4 кДж/моль.
Рассмотрим механизм этой реакции:
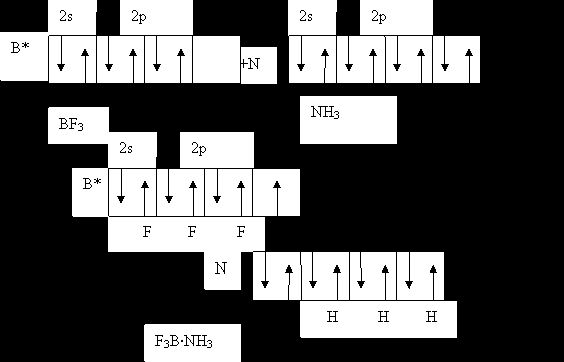 Видно, что из четырех орбиталей бора три
заселены, а одна - остается вакантной. В молекуле аммиака заселены все четыре
орбитали азота, из них три – по обменному механизму электронами азота и
водорода, а одна содержит электронную пару, оба электрона которой принадлежат
азоту. Такая электронная пара называется неподеленной электронной парой.
Образование соединения H3N · BF3 происходит за счет того, что неподеленная
электронная пара аммиака занимает вакантную орбиталь фторида бора. При этом
уменьшается потенциальная энергия системы и выделяется эквивалентное количество
энергии. Подобный механизм образования называют донорно-акцепторным, донором –
такой атом, который отдает свою электронную пару для образования связи (в
данном случае атом азота); а атом, который предоставляя вакантную орбиталь, принимает электронную пару, называется акцептором (в данном случае атом бора).
Донорно-акцепторная связь является разновидностью ковалентной связи.
Видно, что из четырех орбиталей бора три
заселены, а одна - остается вакантной. В молекуле аммиака заселены все четыре
орбитали азота, из них три – по обменному механизму электронами азота и
водорода, а одна содержит электронную пару, оба электрона которой принадлежат
азоту. Такая электронная пара называется неподеленной электронной парой.
Образование соединения H3N · BF3 происходит за счет того, что неподеленная
электронная пара аммиака занимает вакантную орбиталь фторида бора. При этом
уменьшается потенциальная энергия системы и выделяется эквивалентное количество
энергии. Подобный механизм образования называют донорно-акцепторным, донором –
такой атом, который отдает свою электронную пару для образования связи (в
данном случае атом азота); а атом, который предоставляя вакантную орбиталь, принимает электронную пару, называется акцептором (в данном случае атом бора).
Донорно-акцепторная связь является разновидностью ковалентной связи.
В соединении H3N · BF3 азот и бор – четырехвалентны. Атом азота повышает свою валентность от 3 до 4 в результате использования неподеленной электронной пары для образования дополнительной химической связи. Атом бора повышает валентность за счет наличия у него свободной орбитали на валентном электронном уровне. Таким образом, валентность элементов определяется не только числом неспаренных электронов, но и наличием неподеленных электронных пар и свободных орбиталей на валентном электронном уровне.
Более простым случаем образования химической связи по донорно-акцепторному механизму является реакция аммиака с ионом водорода:
![]() . Роль
акцептора электронной пары играет пустая орбиталь иона водорода. В ионе аммония
NH4+ атом азота четырехвалентен.
. Роль
акцептора электронной пары играет пустая орбиталь иона водорода. В ионе аммония
NH4+ атом азота четырехвалентен.
Направленность связей и гибридизация атомных орбиталей
Важной характеристикой молекулы, состоящей более чем из двух атомов, является ее геометрическая конфигурация. Она определяется взаимным расположением атомных орбиталей, участвующих в образовании химических связей.
Перекрывание электронных облаков возможно только при определенной взаимной ориентации электронных облаков; при этом область перекрывания располагается в определенном направлении по отношению к взаимодействующим атомам.
При образовании ионной связи электрическое поле иона обладает сферической симметрией и поэтому ионная связь не обладает направленностью и насыщаемостью.
NaCl CsCl
к.ч. = 6 к.ч. = 6
Угол между связями в молекуле воды составляет 104,5о. Величину его можно объяснить на основании квантово-механических представлений. Электронная схема атома кислорода 2s22p4. Две неспаренные p-орбитали расположены под углом 90о друг к другу - максимум перекрывания электронных облаков s-орбиталей атомов водорода с p-орбиталями атома кислорода будет в том случае, если связи расположены под углом 90о. В молекуле воды связь О – Н полярна. На атоме водорода эффективный положительный заряд δ+, на атоме кислорода - δ-. Поэтому увеличение угла между связями до 104,5о объясняется расталкиванием эффективных положительных зарядов атомов водорода, а также электронных облаков.
Электроотрицательность серы значительно меньше, чем ЭО кислорода. Поэтому полярность связи H –S в H2S меньше полярности связи Н–О в Н2О, а длина связи H–S (0,133 нм) больше, чем Н–О (0,56 нм) и угол между связями приближается к прямому. Для H2S он составляет 92о, а для H2Se – 91o.
По этим же причинам молекула аммиака имеет пирамидальное строение и угол между валентными связями H–N–H больше прямого (107,3о). При переходе от NH3 к PH3, AsH3 и SbH3 углы между связями составляют соответственно 93,3о; 91,8о и 91,3о.
Гибридизация атомных орбиталей
Возбужденный атом бериллия имеет конфигурацию 2s12p1, возбужденный атом бора - 2s12p2 и возбужденный атом углерода - 2s12p3. Поэтому можно считать, что в образовании химических связей могут участвовать не одинаковые, а различные атомные орбитали. Например, в таких соединениях как BeCl2, BeCl3,CCl4 должны быть неравноценные по прочности и направлению связи, причем σ-связи из p-орбиталей должны быть более прочными, чем связи из s-орбиталей, т.к. для p-орбиталей имеются более благоприятные условия для перекрывания. Однако опыт показывает, что в молекулах, содержащих центральные атомы с различными валентными орбиталями (s, p, d), все связи равноценны. Объяснение этому дали Слейтер и Полинг. Они пришли к выводу, что различные орбитали, не сильно отличающиеся по энергиям, образуют соответствующее число гибридных орбиталей. Гибридные (смешанные) орбитали образуются из различных атомных орбиталей. Число гибридных орбиталей равно числу атомных орбиталей, участвующих в гибридизации. Гибридные орбитали одинаковы по форме электронного облака и по энергии. По сравнению с атомными орбиталями они более вытянуты в направлении образования химических связей и поэтому обусловливают лучшее перекрывание электронных облаков.
Рекомендуем скачать другие рефераты по теме: ответы на сканворды в одноклассниках, реферат условия.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 9 | Следующая страница реферата