
Химическая связь. Типы взаимодействия молекул
Категория реферата: Биология и химия
Теги реферата: зимой сочинение, новшество
Добавил(а) на сайт: Федосия.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 9 | Следующая страница реферата
Гибридизация атомных орбиталей требует затрат энергии, поэтому гибридные орбитали в изолированном атоме неустойчивы и стремятся превратиться в чистые АО. При образовании химических связей гибридные орбитали стабилизируются. Вследствие более прочных связей, образованных гибридными орбиталями, из системы выделяется больше энергии, и поэтому система становится более стабильной.
sp–гибридизация имеет место, например, при образовании галогенидов Be, Zn, Co и Hg (II). В валентном состоянии все галогениды металлов содержат на соответствующем энергетическом уровне s и p-неспаренные электроны. При образовании молекулы одна s- и одна р-орбиталь образуют две гибридные sp-орбитали под углом 180о.
Экспериментальные данные показывают, что все галогениды Be, Zn, Cd и Hg (II) линейны и обе связи имеют одинаковую длину.
sp2-гибридизация. В результате гибридизации одной s-орбитали и двух p-орбиталей образуются три гибридные sp2-орбитали, расположенные в одной плоскости под углом 120о друг к другу.
sp3-гибридизация характерна для соединений углерода. В результате гибридизации одной s-орбитали и трех р-орбиталей образуются четыре гибридные sp3-орбитали, направленные к вершинам тетраэдра с углом между орбиталями 109,5о.
Гибридизация проявляется в полной равноценности связей атома углерода с другими атомами в соединениях, например, в CH4, CCl4, C(CH3)4 и др.
В гибридизацию могут включаться не только s- и р-, но и d- и f-орбитали.
При sp3d2-гибридизации образуется 6 равноценных облаков. Она наблюдается в таких соединениях как [SiF6], [Fe(CN)6].
Представления о гибридизации дают возможность понять такие особенности строения молекул, которые не могут быть объяснены другим способом.
Гибридизация атомных орбиталей (АО) приводит к смещению электронного облака в направлении образования связи с другими атомами. В результате области перекрывания гибридных орбиталей оказываются больше, чем для чистых орбиталей и прочность связи увеличивается.
Поляризуемость и поляризующее действие ионов и молекул
В электрическом поле ион или молекула деформируются, т.е. в них происходит относительное смещение ядер и электронов. Такая деформируемость ионов и молекул называется поляризуемостью. Поскольку наименее прочно в атоме связаны электроны внешнего слоя, то они испытывают смещение в первую очередь.
Поляризуемость анионов, как правило, значительно выше поляризуемости катионов.
При одинаковой структуре электронных оболочек поляризуемость иона уменьшается по мере увеличения положительного заряда, например, в ряду:
![]()
Для
ионов электронных аналогов поляризуемость увеличивается с ростом числа
электронных слоев, например: ![]() или
или ![]() .
.
Поляризуемость молекул определяется поляризуемостью входящих в них атомов, геометрической конфигурацией, количеством и кратностью связей и др. Вывод об относительной поляризуемости возможен лишь для аналогично построенных молекул, различающихся одним атомом. В этом случае о различии в поляризуемости молекул можно судить по различию в поляризуемости атомов.
Электрическое поле может быть создано как заряженным электродом, так и ионом. Таким образом, ион сам может оказывать поляризующее действие (поляризацию) на другие ионы или молекулы. Поляризующее действие иона возрастает с увеличением его заряда и уменьшением радиуса.
Поляризующее действие анионов, как правило, значительно меньше, чем поляризующее действие катионов. Это объясняется большими размерами анионов по сравнению с катионами.
Молекулы обладают поляризующим действием в том случае, если они полярны; поляризующее действие тем выше, чем больше дипольный момент молекулы.
Поляризующая
способность увеличивается в ряду ![]() , т.к. радиусы
увеличиваются и электрическое поле, создаваемое ионом, уменьшается.
, т.к. радиусы
увеличиваются и электрическое поле, создаваемое ионом, уменьшается.
Водородная связь
Водородная связь является особым видом химической связи. Известно, что соединения водорода с сильно электроотрицательными неметаллами, такими как F, О, N, имеют аномально высокие температуры кипения. Если в ряду Н2Тe – H2Se – H2S температура кипения закономерно уменьшается, то при переходе от H2S к Н2О наблюдается резкий скачок к увеличению этой температуры. Такая же картина наблюдается и в ряду галогенводородных кислот. Это свидетельствует о наличии специфического взаимодействия между молекулами Н2О, молекулами HF. Такое взаимодействие должно затруднять отрыв молекул друг от друга, т.е. уменьшать их летучесть, а, следовательно, повышать температуру кипения соответствующих веществ. Вследствие большой разницы в ЭО химические связи H–F, H–O, H–N сильно поляризованы. Поэтому атом водорода имеет положительный эффективный заряд (δ+), а на атомах F, O и N находится избыток электронной плотности, и они заряжены отрицательно (d-). Вследствие кулоновского притяжения происходит взаимодействие положительно заряженного атома водорода одной молекулы с электроотрицательным атомом другой молекулы. Благодаря этому молекулы притягиваются друг к другу (жирными точками обозначены водородные связи).
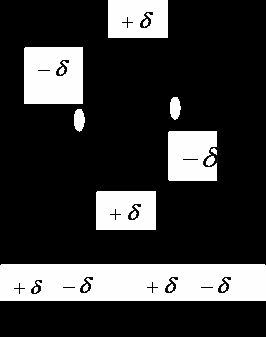
Водородной называется такая связь, которая образуется посредством атома водорода, входящего в состав одной из двух связанных частиц (молекул или ионов). Энергия водородной связи (21–29 кДж/моль или 5–7 ккал/моль) приблизительно в 10 раз меньше энергии обычной химической связи. И тем не менее, водородная связь обусловливает существование в парах димерных молекул (Н2О)2, (HF)2 и муравьиной кислоты.
В ряду сочетаний атомов НF, HO, HN, HCl, HS энергия водородной связи падает. Она также уменьшается с повышением температуры, поэтому вещества в парообразном состоянии проявляют водородную связь лишь в незначительной степени; она характерна для веществ в жидком и твердом состояниях. Такие вещества как вода, лед, жидкий аммиак, органические кислоты, спирты и фенолы, ассоциированы в димеры, тримеры и полимеры. В жидком состоянии наиболее устойчивы димеры.
Межмолекулярные взаимодействия
Ранее рассматривались связи, обусловливающие образование молекул из атомов. Однако между молекулами также существует взаимодействие. Оно является причиной конденсации газов и превращения их в жидкие и твердые тела. Первую формулировку силам межмолекулярного взаимодействия дал в 1871 г. Ван-дер-Ваальс. Поэтому они получили название вандерваальсовых сил. Силы межмолекулярного взаимодействия можно подразделить на ориентационные, индукционные и дисперсионные.
Рекомендуем скачать другие рефераты по теме: ответы на сканворды в одноклассниках, реферат условия.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 9 | Следующая страница реферата