
Эволюция энергетических процессов у эубактерий
Категория реферата: Рефераты по науке и технике
Теги реферата: антикризисное управление предприятием, большие рефераты
Добавил(а) на сайт: Arkadij.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 9 10 11 | Следующая страница реферата
Другие реакции субстратного фосфорилирования ограничены какими-либо специфическими видами брожения. Например, сбраживание некоторых пиримидинов и аргинина, осуществляемое отдельными видами бактерий из рода Streptococcus, приводит к образованию карбамоилфосфата, фосфатная группа которого переносится на АДФ в реакции, катализируемой карбаматкиназой:
карбамоилфосфат + АДФ ® карбамат + АТФ.
Один вид клостридиев (C. cylindrosporum), сбраживающий пурины, способен образовывать формиат и тетрагидрофолат (ТГФК) из формилтетрагидрофолиевой кислоты в реакции, сопровождающейся фосфорилированием АДФ:
формил-ТГФК + АДФ + ФН ® формиат + ТГФК + АТФ.
Для этого вида указанная реакция служит основным путем получения АТФ.
Все реакции субстратного фосфорилирования локализованы в цитозоле клетки. Это указывает на простоту химических механизмов, лежащих в основе субстратного фосфорилирования.
Проблема акцептора электронов
Основная проблема всех процессов брожения — проблема акцептора электронов. В конечном итоге степень окисления и сопряженное с этим количество свободной энергии, а также характер образующихся продуктов определяются природой конечных акцепторов электронов. При брожениях конечными акцепторами электронов служат в основном органические соединения: метаболиты, образующиеся из исходных субстратов (пировиноградная кислота, ацетальдегид), или вещества, имеющиеся в среде культивирования (некоторые аминокислоты и другие органические соединения, способные восстанавливаться). В ряде брожений акцепторами электронов служат молекулы CO2, а также ионы водорода (H2). Кроме того, в отдельных случаях дополнительными акцепторами электронов могут быть некоторые достаточно окисленные неорганические соединения, такие как нитрат, молекулярная сера. Если конечным акцептором электронов является ацетальдегид, образуется этанол, если пируват — молочная кислота. Акцептирование электронов молекулами CO2 приводит у разных видов к возникновению формиата или ацетата, если же эту функцию выполняют ионы водорода, образуется молекулярный водород (H2).
Восстановленные соединения, акцептировавшие электроны, выделяются из клеток эубактерий в окружающую среду и накапливаются в ней в значительных количествах. Из-за низкого энергетического выхода процессов брожения для обеспечения энергией всех функций и биосинтетических процессов клетке приходится перерабатывать огромные количества субстратов.
Итак, брожение — это способ получения энергии, при котором АТФ образуется в процессе анаэробного окисления органических субстратов в реакциях субстратного фосфорилирования.
ГОМОФЕРМЕНТАТИВНОЕ МОЛОЧНОКИСЛОЕ БРОЖЕНИЕ
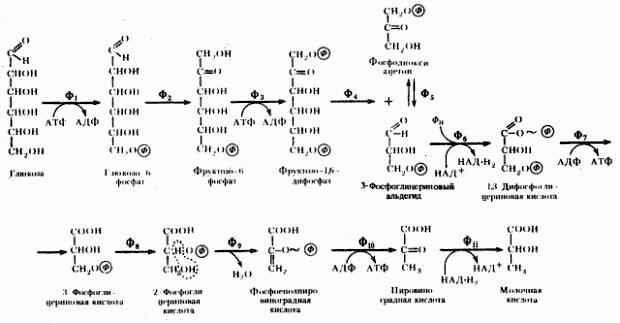
Последовательность биохимических реакций, лежащих в основе гомоферментативного молочнокислого брожения, получила название гликолитического пути (гликолиза)41, фруктозодифосфатного пути, или пути Эмбдена — Мейергофа — Парнаса (Н. Embden, О. Meyerhof, Я. О. Парнас), по именам исследователей, внесших больший вклад в изучение этого процесса. Общая схема гомоферментативного молочнокислого брожения представлена на рис. 53.
|
| Рис. 53. Гомоферментативное молочнокислое брожение: Ф1 — гексокиназа; Ф2 — глюкозофосфатизомераза; Ф3 — фофсофруктокиназа; Ф4 — фруктозо-1,6-дифосфатальдолаза; Ф5 — триозофосфатизомераза; Ф6 — 3-ФГА-дегидрогеназа; Ф7 — фофсоглицерокиназа; Ф8 — фосфоглицеромутаза; Ф9 — енолаза; Ф10 — пируваткиназа; Ф11 — лактатдегиброгеназа (по Dagley, Nicholson, 1973) |
Основными энергетическими ресурсами для эубактерий, осуществляющих гомоферментативное молочнокислое брожение, служат моносахара (в первую очередь, глюкоза) и дисахара (мальтоза, лактоза). В процессе подготовки к энергетическим преобразованиям дисахара ферментативным путем расщепляются до моносахаров. Различные моносахара, прежде чем подвергнуться преобразованиям, должны превратиться в глюкозо-6-фосфат. Момент унификации, т. е. превращения различных субстратов в один, исходный для дальнейшего его метаболизирования по данному пути, очень важен. От того, что служит исходным энергетическим ресурсом, зависит общий энергетический баланс процесса.
41 Собственно гликолиз — это определенная последовательность ферментативных реакций от углевода до пировиноградной кислоты, поэтому, строго говоря, "гликолиз" не является синонимом "гомоферментативного молочнокислого брожения", но 10 из 11 реакций у этих процессов идентичны.
Если исходным энергетическим субстратом служит глюкоза, первое превращение, которому она подвергается, — фосфорилирование. В результате образуется глюкозо-6-фосфат — метаболически активная форма глюкозы. Если исходный энергетический субстрат — лактоза, первым шагом на пути метаболизирования является ферментативное расщепление лактозы с помощью (3-галактозидазы на D-галактозу и D-глюкозу. D-галактоза затем подвергается фосфорилированию, приводящему к образованию D-галактозо-1-фосфата. Последний подвергается серии ферментативных превращений с участием УТФ в качестве кофермента, в результате которых превращается в глюкозо-1-фосфат.
У некоторых бактерий из рода Lactobacillus имеется фермент мальтозофосфорилаза, катализирующий реакцию:
мальтоза + H3PO4 ® глюкозо-1-фосфат + глюкоза.
В результате этой реакции осуществляется расщепление дисахарида мальтозы на две молекулы глюкозы, одна из которых образуется в фосфорилированной форме. Здесь важно подчеркнуть, что в этой реакции молекула фосфорилированной глюкозы синтезируется без затраты АТФ.
Если исходным энергетическим субстратом, вовлекаемым в процесс гликолиза, служит полисахарид типа гликогена или крахмала, его использование начинается с фосфоролитического отщепления глюкозного остатка, протекающего по схеме:
(глюкоза)n + HPO42 – ® (глюкоза)n – 1 + глюкозо-1-фосфат.
Глюкозо-1-фосфат, образующийся в результате подготовительных превращений углеводов, иных, чем глюкоза, превращается затем в глюкозо-6-фосфат. Перемещение фосфатной группы из положения 1 в положение 6 катализируется ферментом фосфоглюкомутазой. Дальнейшее превращение глюкозо-6-фосфата одинаково независимо от исходного энергетического субстрата (рис. 53).
Молекула глюкозо-6-фосфата изомеризуется в молекулу фруктозо-6-фосфата. Последний фосфорилируется в положении 1. Донором фосфата служит АТФ. Вторичное фосфорилирование молекулы фруктозы приводит к ее дальнейшему активированию.
Образовавшийся фруктозо-1,6-дифосфат разрывается на две триозы: фосфодиоксиацетон и 3-ФГА. Разрыв катализируется фруктозо-1,6-дифосфатальдолазой (альдолазой), являющейся ключевым ферментом этого пути. Достаточно обнаружить альдолазу, чтобы получить свидетельство существования гликолитического пути у организма. В последующие реакции может включаться только 3-ФГА. Фосфодиоксиацетон превращается в 3-ФГА в реакции изомеризации, катализируемой триозофосфатизомеразой.
На этом этапе заканчивается подготовительная стадия гликолитического пути: молекула глюкозы после активирования и расщепления на 2 фосфотриозы подготовлена для последующих превращений. Для активирования 1 молекулы глюкозы тратятся 2 молекулы АТФ42. Таким образом, до сих пор процесс протекает с затратой энергии. Однако его смысл и назначение заключаются в обеспечении клетки энергией. Эта задача решается на следующей стадии.
Окисление 3-ФГА до 1,3-дифосфоглицериновой кислоты — один из наиболее важных этапов гликолитического пути, поскольку именно на этом этапе энергия, освобождающаяся при окислении альдегидной группы 3-ФГА, запасается в молекуле 1,3-ФГК. Реакция катализируется ферментом 3-ФГА-дегидрогеназой:
Рекомендуем скачать другие рефераты по теме: реферат реформы, экзамен.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 9 10 11 | Следующая страница реферата