
Галогены
Категория реферата: Рефераты по науке и технике
Теги реферата: бесплатные курсовые работы, характеристика реферата
Добавил(а) на сайт: Агапия.
1 2 3 4 | Следующая страница реферата

 |
Галогены
Всем известно, что фтор вводят в состав зубной пасты, а хлором дезинфицируют воду в плавательных бассейнах. Бром применяют в качестве успокоительного средства, а спиртовой раствор йода как антисептическое средство. Фтор, хлор, бром и йод образуют семейство галогенов. Галогены относятся к неметаллическим элементам. Они входят в VII группу периодической системы (см. рис.).
 |
О происхождении названий галогенов
Названия всех галогенов, за исключением фтора, происходят от греческих слов:
| Название | Исходное слово | Значение |
| Галоген | галс (греч.) ген (греч.) | Соль Образующий |
| Фтор | флуо (лат.) | Течь, текучий (в старину минерал полевой шпат CaF, использовали в металлургии в качестве флюса для придания легкоплавкости шлакам) |
| Хлор | хлорос (греч.) | Зеленовато-желтый |
| Бром | бромос (греч.) | Зловонный |
| Иод | иодес (греч.) | Фиолетовый |
| Астат | астатос (греч.) | Неустойчивый |
Слог «ген» в качестве приставки либо суффикса входит во многие научные термины, например в слова генератор и антиген. Обычно он означает рост или образование чего-либо. Таким образом, слово галоген (гало + ген) означает «образующий соль».
ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
Атомы всех галогенов имеют во внешней оболочке семь электронов. Они легко присоединяют еще один электрон, образуя галогенидные ионы. Галогенид-ион имеет устойчивый октет электронов. Галогены характеризуются высокой электроотрицательностью и реакционной способностью и поэтому в свободном виде не встречаются в природе. Однако галогенид-ионы широко распространены в природе.
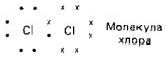
Галогены в свободном виде существуют в форме двухатомных молекул. Атомы в этих молекулах связаны между собой простой ковалентной связью. Каждая такая связь образуется в результате обобществления пары электронов - по одному от каждого атома:
В табл. 1 приведены некоторые данные о структуре атомов и молекул галогенов. Обратим внимание на то, что атомные и ионные радиусы галогенов, а также длины связи в их молекулах последовательно возрастают при перемещении к нижней части группы. Однако энергии диссоциации связи и, следовательно, прочность связи в молекулах галогенов при этом, наоборот, уменьшаются. Исключением в этом отношении является только фтор. Небольшая прочность связи фтора, по-видимому, обусловлена слишком близким расположением атомов в его молекуле. Это приводит к сильному отталкиванию между несвязывающими электронами, что вызывает ослабление связи.
Таблица 1. Электронное строение и свойства галогенов
| Элемент | Атомный номер | Электронная конфигурация атомов | Конфигурация внешней оболочки | Атомный радиус, нм | Ионный радиус, нм | Длина связи, нм | Энергия диссоциации связи, кДж/моль |
| Фтор | 2.7 | 2s22p5 | 0,072 | 0,136 | 0,142 | 158 | |
| Хлор | 17 | 2.8.7 | Зs23p5 | 0,099 | 0,181 | 0,200 | 242 |
| Бром | 35 | 2.8.18.7 | 4s24р5 | 0,114 | 0,195 | 0,229 | 193 |
| Иод | 53 | 2.8.18.18.7 | 5s25р5 | 0,133 | 0,216 | 0,266 | 151 |
ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
Хлор. Хлор можно получить в лабораторных условиях окислением концентрированной соляной кислоты манганатом(VII) калия:
![]()
Выделяющийся хлор пропускают через воду, чтобы удалить следы хлороводородов, а затем через концентрированную серную кислоту, чтобы осушить его. Полученный хлор собирают в перевернутом сосуде, из которого он вытесняет воздух.
Другой способ лабораторного получения хлора основан на реакции между отбеливающим порошком (гипохлоритом кальция) и разбавленной соляной кислотой:
![]()
Бром. Для получения брома в лабораторных условиях добавляют оксид марган-Ha(IV) к смеси концентрированной серной кислоты с бромидом калия. Бромоводород-ная кислота, обоазуюшаяся в оеакции между сеоной кислотой и бромидом калия:
![]()
окисляется оксидом марганца(IV)
![]()
Бром отделяют от реакционной смеси перегонкой.
Иод. Иод получают тем же способом, что и бром, только вместо бромида калия используется иодид калия. Полученный иод отделяют от реакционной смеси возгонкой.
ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
Рекомендуем скачать другие рефераты по теме: русский язык 9 класс изложения, реферат современная россия.
1 2 3 4 | Следующая страница реферата