
Синтез хлорида олова (IV)
Категория реферата: Биология и химия
Теги реферата: доклад по обж, реферат
Добавил(а) на сайт: Majsak.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата
Второй способ.
Собирают прибор согласно схеме (рис. 4.22).
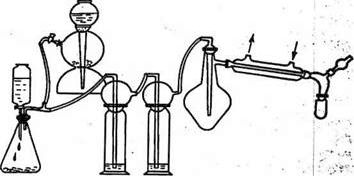
Рис. 5. Прибор для получение хлорида олова (IV).
Все части прибора должны быть тщательно высушены . В реакционную колбу помещают определенное количество металлического олова, заполняют прибор углекислым газом, колбу нагревают до плавления олова и пропускают в нее ток сухого очищенного хлора. Дальнейшее нагревание продолжают в том случае, если реакция замедляется.
Sn + 2Cl2 = SnCl4
По окончании реакции из системы вытесняют хлор сухим углекислым газом. Выход продукта оценивают по объему и плотности полученного вещества. Часть хлорида олова (IV) отгоняют в пробирку с оттянутым концом, которую затем запаивают, или в пробирку которую закрывают пробкой и парафинируют. Оставшуюся часть продукта используют для изучения его свойств.
Третий способ.
Безводный препарат можно получить также хлорированием безводного SnCl2
SnCl2 + Cl2 = SnCl4
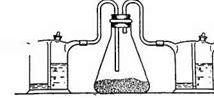
Рис. 6. Прибор для получения хлорного олова из SnCl2
В коническую колбу (рис. 5) помещают 200 г безводного SnCl2 и пропускают (под тягой) струю хлора со скоростью 60—70 пузырьков в минуту. Хлор предварительно пропускают через склянку Тищенко с конц. H2SO4. Избыток хлора поглощается в другой склянке Тищенко с раствором NaOH. Реакция протекает с сильным разогреванием реакционной смеси (до 70—80 оС) и вскоре кристаллическая масса SnCl2 превращается в жидкость (SnCl4). Конец реакции определяется по постепенному снижению температуры. Полученную жидкость переливают в колбу для перегонки, добавляют немного листового олова для связывания растворенного хлора и медленно перегоняют, собирая фракцию, кипящую при 112—114 оС.
Выход 250 г (90%).
На основании анализа литературных данных и исходя из наших возможностей, для получения тетрахлорида олова использовали метод, основанный на непосредственном взаимодействии олова с хлором (второй способ).
Экспериментальная часть.
1. Синтез тетрахлорида олова.
|
Вещество |
Молярная масса, М г/моль |
Масса m, г |
Кол-во вещества, ν моль |
Физические константы |
|
|
mтеор |
mпракт |
νтеор |
νпракт |
||
|
Олово |
119 Рекомендуем скачать другие рефераты по теме: шпоры по менеджменту, реферат чрезвычайные ситуации. Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата Поделитесь этой записью или добавьте в закладкиКатегории: |